近日,同心医疗全资子公司BrioHealth Solutions, Inc.完成了公司自主研发的全磁悬浮左心室辅助装置BrioVAD美国INNOVATE临床试验安全性阶段的植入工作,实现了又一重要里程碑。这标志着该试验安全性阶段30天随访工作的全面启动,并将在数据收集完成后递交美国食品药品监督管理局(FDA),以便进入确证性阶段。同时,公司正在加速确证性阶段的各项筹备工作;根据INNOVATE临床试验的设计方案,在进入确证性阶段后,入组中心数量允许扩展至60家。

关于BrioVAD系统
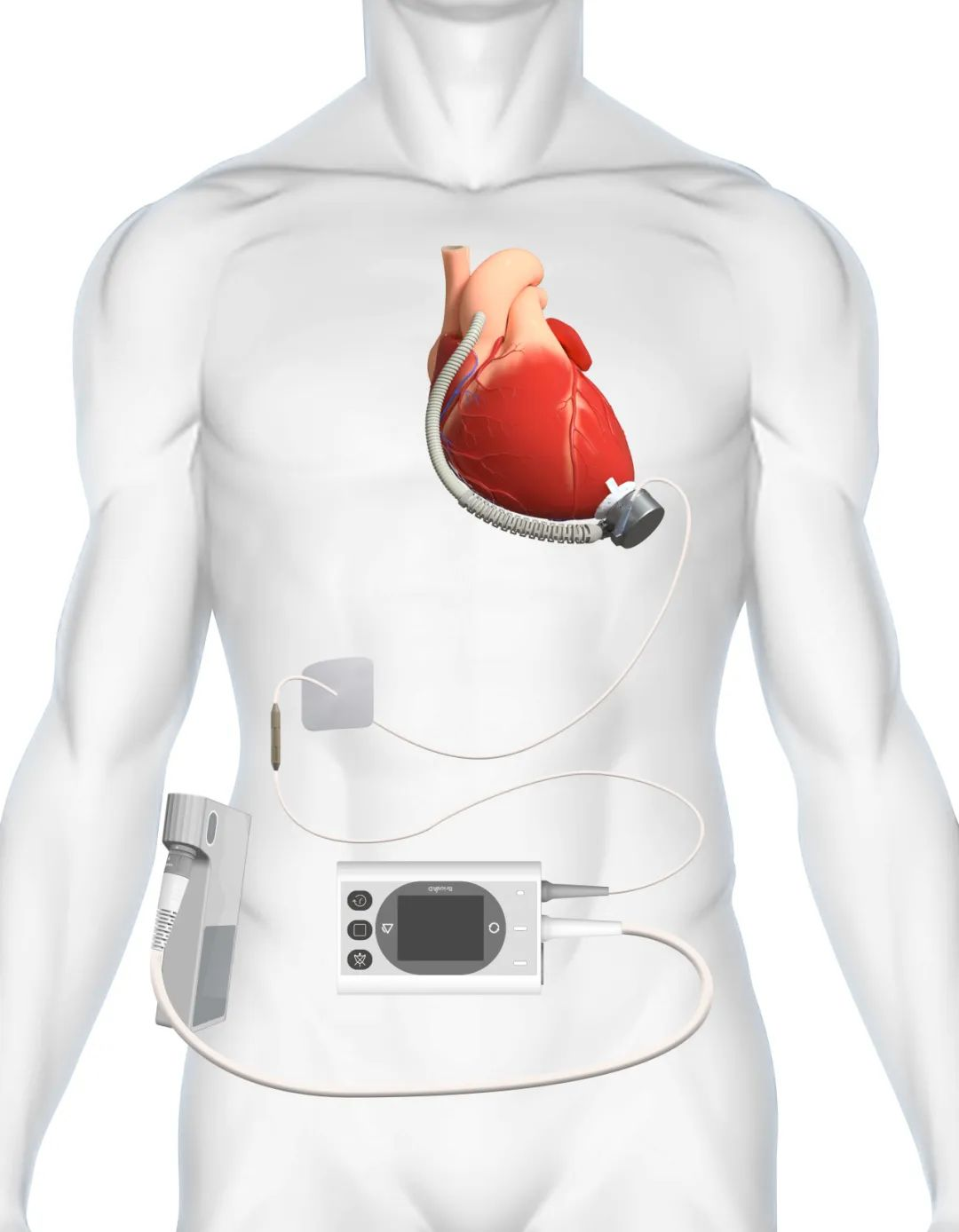
BrioVAD系统示意图

BrioVAD系统主要部件
BrioVAD系统是一种能提供全流量支持的耐久型VAD,由可植入的血泵和外部组件组成,旨在为心衰患者提供长期支持。与目前唯一获得美国FDA批准的耐久型VAD相比,BrioVAD血泵采用了创新的分立式磁悬浮设计,实现了更小泵体与大叶轮的完美结合,有助于减少手术创伤。此外,BrioVAD还采用了创新的经皮电缆设计,更细、更柔软的经皮电缆有助于降低相关的感染风险。
BrioVAD血泵独特的磁悬浮结构和大直径叶轮也为泵内流道的优化提供了基础。先进的流道设计有助于有提升设备的血液相容性和血流动力学性能,从而降低严重并发症的风险。
BrioVAD系统的外部组件采用了多项独特设计,患者日常仅需佩戴两个组件,有助于提升用户体验和患者的生活质量。
关于INNOVATE临床试验

INNOVATE是一项前瞻性、随机对照、非盲、多中心、确证性临床试验,将招募短期和长期机械循环支持适应症的患者,旨在评估BrioVAD系统在治疗晚期、难治性心力衰竭方面的安全性和有效性。该试验的参与者以2:1的比例随机接受BrioVAD或HeartMate 3,主要终点指标是短期(6个月)和长期(24个月)免于致残性卒中和泵置换的生存率。其他终点指标包括评估心力衰竭患者的不良事件、心功能和生活质量。研究还将验证植入BrioVAD是否能减少随访期内的总住院天数。该试验预计将在美国领先的医疗中心招募约800名患者。有关更多信息,可访问www.theinnovatetrial.com。
2023年8月7日,《人民日报》发表题为《国产全磁悬浮人工心脏服务患者》的报道,对同心医疗打破国际技术垄断,研发出自主知识产权的全磁悬浮人工心脏表示肯定。目前该产品已经覆盖全国近40家医院,让140多名终末期心衰患者开启了“心”生活。
近日,在被誉为医学界最高级别大会的“2022中国医学发展大会”上,中国医学科学院发布了《中国21世纪重要医学成就》和《中国2021年度重要医学进展》。作为全球VAD领域的技术突破者,同心医疗自主研发的“慈孚植入式左心室辅助系统获批上市”(国械注准20213120987)入选《中国2021年度重要医学进展》。
2021年11月24日,同心医疗自主研发的CH-VAD植入式左心室辅助系统正式获得国家药品监督管理局(NMPA)批准上市(注册证号:国械注准20213120987)。这是我国首个获得NMPA批准的拥有完备自主知识产权的国产人工心脏,也是全球范围内首个获得NMPA批准的全磁悬浮式人工心脏,标志着全球新一代技术路线(全磁悬浮技术路线)的心室辅助装置产品在中国商业化落地。

